多囊卵巢会影响试管受精卵着床吗?激素内膜都有影响
多囊卵巢综合症作为育龄期女性常见的内分泌疾病,其复杂的代谢异常确实可能影响试管受精过程中胚胎着床的成功率。现代生殖医学研究证实,这类患者子宫内膜容受性改变、胰岛素抵抗及慢性炎症状态,共同构成影响胚胎植入的潜在风险网络。通过精准的激素调控与代谢干预,可使着床成功率提升至与健康人群相当水平。
多囊卵巢导致激素失衡影响生育
高雄激素水平如同扰乱生理节律的噪声。多囊患者卵巢产生的过量雄激素,不仅抑制卵泡正常发育,还会改变子宫内膜基因表达谱。研究发现,这类患者的子宫内膜在胚胎着床窗口期,整合素β3等关键黏附分子的表达量下降约40%,相当于为胚胎安置设置了分子级别的障碍。
促黄体生成素(LH)的持续性分泌异常。正常月经周期中LH峰是触发排卵的关键信号,但多囊患者的LH基线水平常高出健康人群2-3倍。这种持续性的激素刺激,会导致子宫内膜过早成熟,使得胚胎进入宫腔时,内膜已错过最佳接纳时机,这种现象在临床称为"种植窗移位"。
多囊卵巢引起代谢紊乱的连锁反应
胰岛素抵抗引发的宫腔微环境改变。约70%的多囊患者存在胰岛素敏感性下降,高胰岛素血症会刺激子宫内膜产生过量纤溶酶原激活物抑制因子-1(PAI-1)。这种物质不仅影响胚胎滋养层细胞的侵袭能力,还会使子宫内膜下血管网络形成受阻,相当于切断了胚胎植入后的营养供给线。
脂肪因子分泌紊乱的隐形影响。多囊患者的脂肪组织异常分泌瘦素、脂联素等信号分子,其中脂联素水平通常降低30%-50%。这种代谢失衡会通过mTOR信号通路干扰子宫内膜细胞的能量代谢,导致胚胎附着阶段基质细胞蜕膜化进程受阻,直接影响胚胎与母体的物质交换效率。
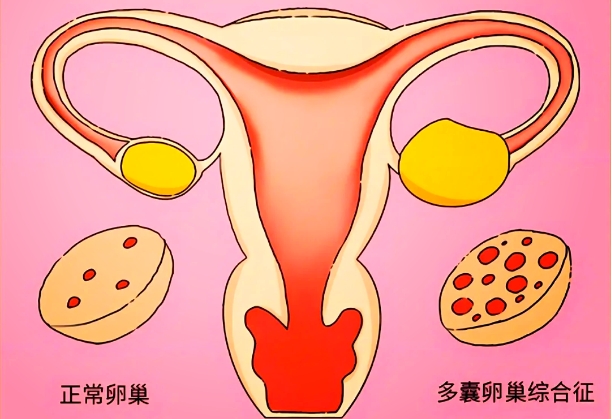
多囊卵巢影响子宫内膜的发育
子宫内膜同步化发育障碍。正常着床需要胚胎发育阶段与内膜成熟度高度匹配,但多囊患者的子宫内膜常存在时钟基因表达紊乱。Per2、Bmal1等调控细胞周期的基因表达波动幅度减少50%,导致内膜上皮与基质细胞发育不同步,如同错位的齿轮难以咬合。
糖蛋白复合物的结构异常。胚胎着床需要子宫内膜表面形成特殊的糖萼结构,但多囊患者的子宫内膜上皮细胞中,MUC1黏蛋白的糖基化修饰发生改变。这种分子结构的细微变化,会使胚胎滋养层细胞无法识别并锚定合适位点,相当于在细胞表面设置了错误的路标。
多囊卵巢的生育治疗方案
二甲双胍的代谢重塑作用。这类胰岛素增敏剂可使多囊患者的胚胎着床率提高18%-25%,其机制不仅是改善糖代谢,还能下调子宫内膜雄激素受体表达,恢复HOXA10等着床相关基因的正常转录。用药3个月后,内膜血管内皮生长因子(VEGF)的表达量可回升至正常水平的85%。
个体化内膜准备方案。针对多囊患者研发的改良激素替代方案,通过延长雌激素暴露时间并精准控制孕酮转化时机,能将种植窗同步率提升至92%。部分医疗中心采用宫腔灌注粒细胞集落刺激因子(G-CSF),可使内膜厚度不足患者的临床妊娠率提高30%。
总之,多囊卵巢综合症对胚胎着床的影响并非不可逾越的障碍,而是需要医患共同解密的生物密码。随着分子诊断技术的发展,现在可通过子宫内膜容受性检测(ERT)精准定位每位患者的最佳移植时机。临床数据显示,经过系统治疗的多囊患者,其试管受精的累积活产率可达65%-70%,与普通不孕症人群差异已缩小至5%以内。
讨论群
与本文相关问答
大家一起在讨论
相关百科
最新百科
热门百科
- 无精症患者还能生育吗?试管婴儿技术详解及应对方案
- B超监测排卵未孕何时考虑试管?试管技术的适应症种类
- 自闭症是父亲的基因造成的?父母年龄双向影响自闭症
- 弱精吃了左卡尼汀3月有效果吗?弱精治疗后的维持情况
- 39岁生二胎的生育选择:自然怀孕还是试管婴儿?
- 多囊卵巢会影响试管受精卵着床吗?激素内膜都有影响
- 精子和卵子质量差还能怀孕吗?精卵质量的改善方法
- 内膜薄宫腔灌注做几次才有效?内膜薄宫腔灌注的时间



